Quality
Management
当社の品質管理を担う専門部署として、品質管理部を設置しています。品質管理部は、治験施設支援業務に係る標準業務手順書をはじめ、各業務別のマニュアル、業務ツールの整備および運用を行っています。また、専門教育(治験施設支援業務の受託および実施に係る教育)を担い、各支店や関連部署と相互連携を図り、全社的な治験施設支援業務の質の向上、均質化に努めています。
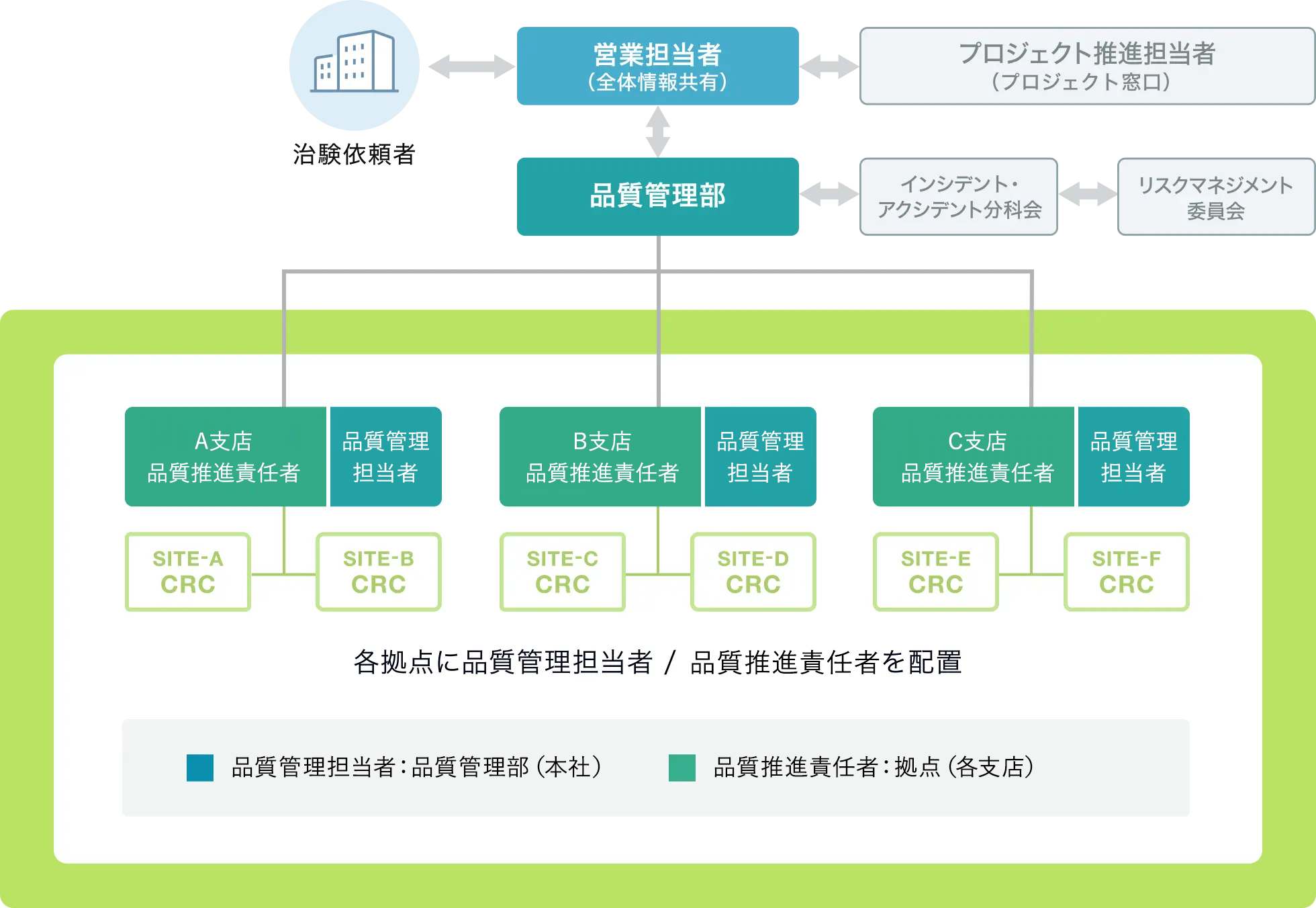
当社では、実施医療機関におけるリスクに基づくプロセス管理を支援、推進し、治験データの品質確保を図っています。
各実施医療機関担当のCRC、SMA(治験事務局担当者)およびBD(施設営業担当者)が、治験担当医師および施設スタッフと協議の上、治験実施体制の構築およびプロセスの構築を支援します。また、品質管理担当者および品質推進責任者が実施医療機関を訪問し、プロセスに従い治験業務が実施されていることを第三者の視点で点検します。
品質管理部において全社のアクシデント情報を報告システムにより一元管理しており、アクシデントが発生した場合には、関係者や関連部署と連携し、迅速かつ適切に対応します。発生後、品質管理部では事故および発生した事故の背景要因等の調査・分析を行い、専門委員会(インシデント・アクシデント分科会)おいて、原因の究明と再発防止策等を検討し、速やかに実施して再発防止に努めています。
当社は、コンプライアンスを重視し、治験データの信頼性確保に取り組んでいます。
